Senyawa organik yang ada dalam protoplasma meliputi:
(1) Protein,
(2) Karbohidrat,
(3) Lipid,
(4) Enzim,
(5) Zat pengatur seperti vitamin, hormon dan
(6) Asam nukleat.
Sumber Gambar : fc09.deviantart.net/fs15/f/2007/086/a/9/Protoplasm_by_KDH.jpg
1. Protein:
[I] Komposisi protein:
Protein (Gr„ proteuo = 1, menempati urutan pertama) adalah rantai asam amino yang dihubungkan oleh ikatan peptida. Protein adalah senyawa organik terpenting yang ditemukan dalam protoplasma dalam satu bentuk atau lainnya. Protein dengan lipid dan air mewakili konstituen utama protoplasma.
Ini terdiri dari С, О, H, dan N, yang dapat membentuk berbagai kombinasi dengan fosfor dalam asam nukleat dan dengan S, Mg, Fe, dll. Molekul protein berukuran besar, terdiri dari ribuan atom. Berat molekul mereka sangat tinggi. Mereka umumnya tetap dalam keadaan koloid.
Mereka adalah polimer asam amino. Saat dipanaskan, protein dipecah menjadi komponennya – asam amino. Susunan karakteristik asam amino dicontohkan dengan adanya gugus amino (—NH 2 ) dan gugus karboksil (—COOH). Gugus amino bersifat basa dan gugus karboksil bersifat asam. Asam amino ditemukan secara bebas di sitoplasma dan merupakan kumpulan asam amino.
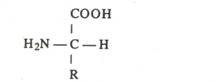
Ini adalah rumus molekul umum asam amino. Di sini NH 2 adalah gugus amino,-COOH adalah gugus karboksil dan R mewakili berbagai kombinasi kimia yang terjadi pada berbagai jenis asam amino.
Asam amino berbeda satu sama lain hanya pada rantai sampingnya, misalnya R pada alanin memiliki satu karbon, sedangkan pada leusin memiliki empat karbon. Sitoplasma mengandung sekitar 22 asam amino. Nama mereka dan formula dari beberapa asam amino diberikan di bawah ini—

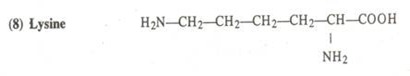
(9) Arginin, (10) Histidin, (11) Serin, (12) Treonin, (13) Sistein, (14) Sistin, (15) Metionin, (16) Fenilalanin, (17) Tirosin, (18) Triptofan, (19) Prolin, (20) Hidroksiprolin, (21) Aspargin, dan (22) Glutamin.
Asam amino dari molekul protein disatukan satu sama lain oleh gugus amino dan karboksil masing-masing, membentuk ikatan atau ikatan peptida. —NH—CO— disebut hubungan peptida atau ikatan peptida. Molekul yang terbentuk mempertahankan karakter amfoternya, karena gugus asam selalu berada di satu ujung dan gugus basa di ujung lainnya, selain residu lateral (radikal) yang dapat bersifat basa atau asam.
Kombinasi dua asam amino adalah dipeptida. Rantai ikatan peptida antara asam amino adalah tulang punggung molekul protein dan struktur utamanya. Biasanya ada 6 jenis asam amino sebagai berikut—
- Asam amino monoamino-monokarboksilat (asam amino sederhana yang memiliki satu gugus karboksil), misalnya glisin (Gly), alanin (Ala), valin (val), leusin (Leu), isoleusin (pengganti).
- Jenis monoamino-dikarboksilat (asam amino asam yang memiliki dua gugus karboksil), misalnya glutamat (Glu), aspartat (Asp).
- Tipe diamino-monokarboksilat (asam amino basa), misalnya arginin (Arg), lisin (Lys), histidin.
- Asam amino aromatik, misalnya tirosin (Tyr), fenilalanin (Phe), atiu triptofan (trip).
- Asam amino yang mengandung sulfur, misalnya methionine (Met), cystine, dan cysteine (Cys).
- Asam amino yang mengandung hidroksil, misalnya treonin (Thr), dan serin (ser).
Selain asam amino di atas ditemukan asam amino lain yang tidak membentuk protein tetapi terjadi sebagai bentuk bebas atau dalam bentuk gabungan lainnya. Ini adalah sebagai berikut seperti yang dijelaskan oleh Mazur dan Harrow (1971) —
(i) β-Alanine adalah konstituen dari karnosin, asam pantotenat, anserin dan otot.
(ii) Citrulline adalah produk antara dalam biosintesis urea.
(iii) Taurin ditemukan dalam garam empedu.
(iv) Kreatin terjadi pada urea.
(v) Phosphoserine ditemukan dalam kasein dan enzim lainnya.
(vi) Ornithine adalah produk perantara dari siklus urea.
(vii) Ergothionine ditemukan dalam ergot dan darah.
(viii) Hydroxylysine terjadi pada kolagen dan embrio anak sapi.
(ix) Homosistein adalah perantara dalam metabolisme metionin.
(x) Cystathionine juga perantara dalam siklus metionin.
(xi) Asam y-Aminobutyric terjadi pada bakteri, ragi, otak, dll.
(xii) Dihidroksifenilalanin adalah produk sampingan dari metabolisme fenilalanin.
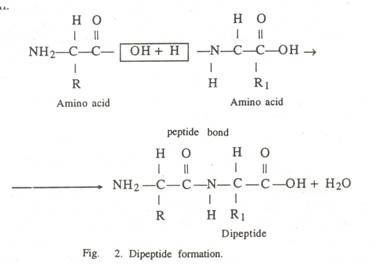
Beberapa asam amino mengandung belerang dengan molekul hidrogennya seperti pada sistin. Kombinasi dua asam amino oleh ikatan peptida disebut sebagai dipeptida, sedangkan kondensasi beberapa atau beberapa asam amino masing-masing disebut oligopeptida dan polipeptida. Berbagai molekul polipeptida bersatu untuk membentuk pepton, protease, dan protein.
[II] Struktur protein:
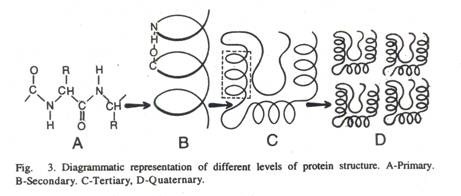
Molekul protein terdiri dari rantai polipeptida yang cukup besar yang tetap terlipat dan hubungan tambahan antara asam amino mereka. Tingkat pelipatan molekul protein menjadikannya struktur yang sangat kompleks. Dengan kata lain, protein menunjukkan tingkat organisasi yang berbeda yaitu primer, sekunder, tersier, dan kuaterner.
- Struktur primer:
Di dalamnya, molekul rantai polipeptida tetap tersusun dalam pola linier tunggal oleh ikatan peptida. Di sini jumlah, sifat dan urutan asam amino dalam rantai polipeptida menentukan struktur primer protein. Struktur primer protein berikut telah ditentukan—
(1) Struktur ribonuklease telah dijelaskan oleh Stein dan rekan kerjanya. Ini memiliki residu 124 asam amino.
(2) Hemoglobin manusia memiliki 574 residu seperti yang dijelaskan oleh Brounitzer dan lainnya.
(3) Sitokrom jantung manusia С terdiri dari 104 asam amino seperti yang diungkapkan oleh Tuppy dan Smith.
(4) Struktur insulin telah dijelaskan oleh Sanger yang terdiri dari dua rantai polipeptida yang disatukan oleh jembatan belerang. Ada 51 asam amino.
- Struktur sekunder:
Ini ditentukan oleh ikatan hidrogen antara oksigen karboksil dan atom hidrogen amida dari asam amino penyusun rantai peptida. Jadi, protein ini memiliki rantai ratusan asam amino yang tersusun secara spiral atau heliks dalam molekulnya. Ikatan (H) dapat terjadi antara rantai polipeptida yang berbeda atau di dalam molekul rantai polipeptida yang sama. Jenis heliks berikut terbentuk di protein sekunder—
(a) α-heliks:
Di dalamnya, rantai peptida berbentuk tangga spiral dengan 3 1/2 molekul asam amino per putaran. Berbagai gulungan heliks disatukan oleh ikatan hidrogen yang terletak sejajar dengan sumbu utama serat. Dengan demikian, a-heliks memberikan fleksibilitas, elastisitas, dan stabilitas pada rantai peptida.
(b) Lembar β-helix atau β-lipit:
Struktur ini melibatkan ikatan hidrogen antara rantai peptida pada sudut kanan ke rantai utama. Jadi, serat β-helix tidak elastis karena rantai polipeptida sudah dalam bentuk memanjang. Namun, struktur tersebut cukup kuat dan fleksibel seperti serat sutra, β-keratin bulu dan cakar.
(c) Kolagen heliks:
Struktur ini lebih rumit dibentuk oleh puntiran tiga heliks rantai polipeptida yang saling terkait satu sama lain sehingga membentuk super heliks tangan kanan. Untai atau rantai rangkap tiga selanjutnya diperkuat oleh ikatan hidrogen antara unit hidroksiprolinnya. Dengan demikian, heliks kolagen adalah struktur yang sangat kuat dan kaku serta tidak dapat dengan mudah dipanjangkan atau ditekuk.
- Struktur tersier:
Di dalamnya, ikatan terjadi antara gugus R asam amino rantai polipeptida yang berdekatan dengan hasil rantai peptida semakin terlipat. Selain itu, rantai ini terlipat sendiri. Berbagai rantai mungkin tetap disatukan oleh ikatan —S—S— dalam
molekulnya. Contoh umum adalah protein globular (albumin, globulin plasma).
- Struktur Kuarter:
Protein ini mengandung dua hingga banyak rantai polipeptida dengan sifat yang sama atau berbeda dan tetap terikat bersama oleh ikatan kovalen yang lemah seperti hemoglobin yang memiliki dua rantai (rantai a dan (α dan β). Protein kuarter mungkin terdiri dari dua jenis.
(i) Dalam satu kategori, molekul protein terdiri dari beberapa rantai peptida yang berbeda tetapi hanya memiliki satu situs aktif.
(ii) Dalam kategori kedua, protein terdiri dari unit-unit yang serupa atau identik.
[III] Klasifikasi protein:
Protein terdiri dari 3 jenis — sederhana, terkonjugasi, dan turunan.
- Protein sederhana:
Ini hanya menghasilkan asam amino atau hidrolisis seperti histon, globulin, albumin, protein sereal (glutenin, oryzein, zein, hordein, gliadin), jaringan hewan (misalnya keratin, elastin, gelatin, kolagen), dan protamine (dari sperma ikan). Mereka terdiri dari dua jenis — (1) protein globular sederhana dan (2) protein berserat sederhana.
- Protein globular sederhana:
Protein ini larut dalam satu atau lebih pelarut dan terbagi dalam dua kategori—
(a) Larut dalam air suling.
(b) Tidak larut dalam air suling.
(a) Larut dalam air suling:
Mereka termasuk tipe-tipe berikut—
(i) Albumin:
Mereka mudah larut dalam air dan dapat diendapkan dari air oleh asam dan basa encer. Lebih kuat atau conc. asam dan basa mengubah albumin menjadi metaprotein yang larut. Saat dipanaskan, mereka terkoagulasi . Contoh umum adalah albumin putih telur, albumin serum, legumelin (protein kacang-kacangan), phaseolin (protein kacang), dan leusin (protein gandum).
(ii) Pseudoglobulin:
Mereka juga larut dalam air dan dapat diendapkan dari air dengan 1/4 sampai 3/4 saturasi dengan garam asam atau amonium sulfat. Tidak seperti albumin, mereka langka di alam dan termasuk pseudoglobulin dari whey susu. Ini dikoagulasi pada pemanasan.
(iii) Protamin:
Ini adalah protein dasar yang sangat larut dalam air, asam encer dan larutan amonium hidroksida encer. Setelah bercampur dengan asam mineral, mereka membentuk garam kristal dan garam yang tidak larut dengan protein yang lebih asam. Mereka tidak dikoagulasi oleh panas dan memiliki berat molekul rendah. Contohnya adalah protein sperma.
(iv) Histon:
Ini adalah protein dasar yang memiliki berat molekul tinggi. Mereka tidak larut dalam amonium hidroksida tetapi larut dalam air dan asam mineral encer. Mereka mungkin terjadi pada nukleoprotein.
(b) Tidak larut dalam air suling:
Di dalamnya, disertakan jenis-jenis berikut—
(i) Gulutelin:
Mereka larut dalam alkali encer dan asam tetapi tidak larut dalam air suling, dan larutan garam netral dan hadir dalam protein sereal, misalnya, glutenin (dari gandum) dan oryzenin (dari beras).
(ii) Gliadin atau Prolamin:
Protein ini juga larut dalam alkali encer dan alkohol 60-80 persen. Prolamin terjadi pada tanaman saja dan termasuk gliadin (gandum), hordein (barley) dan zein (jagung).
(iii) Globulin:
Mereka tidak larut dalam air tetapi mudah larut dalam larutan garam netral encer. Saat dipanaskan, mereka dikoagulasi dan termasuk vitellin (globulin telur), fibrinogen (protein darah), myosinogen (protein otot), dll. Globulin nabati terdiri dari tuberin (kentang), edestin (gandum) dan legumin (gandum).
- Protein berserat sederhana:
Mereka terlihat seperti serat dan tidak larut dalam air dingin atau reagen dingin. Mereka ditemukan secara eksklusif pada hewan dan dikenal sebagai skleroprotein. Beberapa bentuk protein berserat adalah sebagai berikut—
(a) Keratin:
Mereka adalah protein yang tidak dapat dicerna yang ditemukan di rambut, bulu, kuku, tanduk, dll.
(b) Elastin:
Ini adalah protein tidak larut yang ditemukan pada tilase mobil elastis kuning , pembuluh darah, dll.
(c) Fibroin:
Ini hadir dalam sutra.
(d) Kolagen:
Ini terjadi pada jaringan ikat berserat putih yaitu tendon, matriks tulang dan tulang rawan.
Di atas protein, dapat dibagi lagi menjadi dua kelompok—
(i) kelompok Keratin-myosin-elastin-fibrinogen dan (ii) jenis Kolagen. Dalam kategori pertama termasuk protein epidermis, rambut, miosin serat otot, dan protein pembekuan. A-keratin rambut mamalia membentuk β-keratin melalui aksi dengan alkali. Analisis sinar-X dari protein keratin-myosin-elastin-fibrinogen bentuk β-(atau diregangkan) menunjukkan bahwa susunan atom tidak spiral tetapi sebagai rantai polipeptida pita berlipit.
Protein kolagen ditemukan di tendon, tulang rawan dan setelah hidrolisis membentuk gelatin. Molekul kolagen adalah asimetris, batang tipis yang sangat panjang dan terdiri dari tiga rantai peptida, masing-masing memiliki prolin, hidroksiprolin, dan glisin.
- Protein terkonjugasi:
Ini terdiri dari protein sederhana yang digabungkan dengan bagian non-protein, biasanya disebut sebagai gugus prostetik (jika adisi bersifat organik) atau kofaktor (jika adisi bersifat anorganik). Misalnya, glikoprotein dan mucopmtein mengandung karbohidrat dan protein dalam molekulnya (misalnya, musin air liur).
Lipoprotein mengandung asam amino dan lipid dalam molekulnya (misalnya, lipovitellin kuning telur, serum, protein otak dan jaringan saraf). Nukleoprotein mengandung asam amino dan asam nukleat dalam molekul (misalnya, protein asam nukleat). Kromoprotein mengandung asam amino dan pigmen dalam molekulnya (misalnya, hemoglobin, hemosianin, flavoprotein, dan sitokrom).
Hemoglobin dan mioglobin mengandung kelompok prostetik heme, senyawa organik yang mengandung besi yang bergabung dengan oksigen. Fosfoprotein mengandung asam amino dan gugus fosfat dalam molekulnya (misalnya kasein), dan metalloprotein mengandung asam amino dan ion logam dalam molekulnya.
- Protein turunan:
Ini terdiri dari protein terkoagulasi dan sebagian protein terhidrolisis, misalnya protease, polipeptida.
2. Karbohidrat:
(L., karbo—batubara: Gr., hydra—air). Ini paling umum dalam protoplasma dan merupakan sumber energi utama untuk semua makhluk hidup. Mereka terdiri dari С, H, dan O. Hidrogen dan oksigen hadir dalam rasio 2: 1 seperti dalam air. Ketika dihidrolisis, mereka membentuk glukosa dan air. Glukosa diubah menjadi glikogen sebagai produk penyimpanan.
Pada tanaman Mei mereka membentuk konstituen penting dari dinding sel dan berfungsi sebagai elemen pendukung. Jaringan hewan memiliki lebih sedikit karbohidrat; yang paling penting adalah glukosa, galaktosa, glikogen dan gula amino serta polimernya.
Karbohidrat utama yang terdapat pada protoplasma terdiri dari 3 macam yaitu monosakarida, oligosakarida dan polisakarida. Dua yang pertama, umumnya dikenal sebagai gula, mudah larut dalam air. Mereka dapat mengkristal dan dengan mudah melewati membran dialisis. Polisakarida tidak mengkristal atau melewati membran.
[I] Monosakarida:
Ini adalah gula sederhana yang memiliki rumus empiris C n (H20) n . Mereka diklasifikasikan dan diberi nama sesuai dengan jumlah atom karbon dalam molekulnya—
- Triosis:
Ini ditandai dengan adanya 3 atom karbon dalam molekulnya seperti gliseraldehida dan dihidroksiaseton.
- Tetrosa:
Mereka memiliki empat atom karbon seperti erythrulose.
- Pentosa:
Ini adalah gula yang memiliki lima atom karbon dan membentuk penyusun utama asam nukleat. Dalam DNA, mereka terjadi sebagai deoksiribosa dan dalam RNA, mereka ditemukan sebagai ribosa. Gula ribosa juga ditemukan di beberapa koenzim seperti NAD, ATP dan CoA.
- Heksosa:
Ini adalah senyawa dari enam atom karbon dan termasuk gula yang paling umum seperti glukosa, fruktosa dan galaktosa. Mereka manis, mudah larut dalam air dan mudah dikristalisasi. Di dalam tubuh, mereka membentuk sumber energi utama dan juga sebagai bahan mentah untuk biosintesis karbohidrat kompleks.
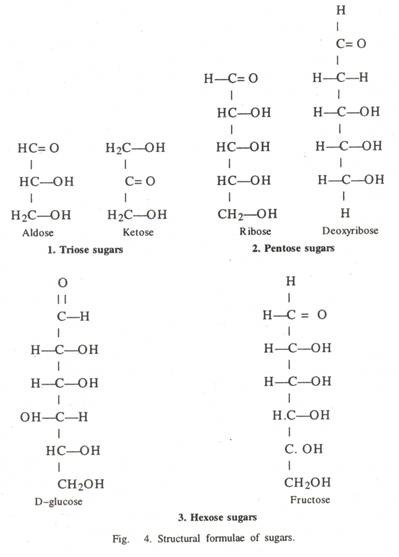
(a) Glukosa:
Ini juga disebut gula anggur atau dekstrosa dan ditemukan dalam buah-buahan, dan dalam madu bersama dengan fruktosa. Dalam air glukosa ada dalam kesetimbangan antara bentuk α dan β. Ini adalah metabolit energi utama dan semua karbohidrat yang diambil dalam makanan akhirnya dipecah menjadi glukosa untuk memulai siklus glikolisis dan kreb.
(b) Fruktosa (levulosa):
Ini juga disebut gula buah atau levulosa dan memiliki komposisi yang mirip dengan glukosa tetapi berbeda sifatnya. Ini kurang mudah dicerna atau diserap daripada glukosa karena posisi gugus OH.
(Ñ ) Galaktosa:
Ini hadir dalam gula susu atau laktosa bersama dengan glukosa. Laktosa akan terurai menjadi glukosa dan galaktosa setelah hidrolisis. Ini mudah diserap seperti glukosa.
Secara struktural, monosakarida dapat dikelompokkan menjadi dua kategori—
(i) Aldosa yang memiliki gugus aldehida (H—C=0) di salah satu ujung rantai dan CH 2 OH di sisi lain.
(ii) Ketosa yang terdiri dari gugus keto (—C=O) pada atom karbon kedua.
- Heptosa:
Ini mengandung tujuh atom karbon dalam molekul mereka, misalnya, sedoheptulosa.
[II] Oligosakarida:
(Gr., oligos, sedikit).
Gula ini dibentuk oleh kondensasi 2 sampai 6 molekul monosakarida yang disebut monomer. Demikian pula, pada hidrolisis, mereka menghasilkan 2-6 molekul monomer atau gula sederhana. Setiap monomer dihubungkan satu sama lain oleh hubungan glikosidik. Atas dasar jumlah monomer, oligosakarida dapat dari jenis berikut—
- Diasakarida:
Ini dibentuk oleh kondensasi dua molekul monomer monosakarida dengan hilangnya satu molekul air. Rumus empiris mereka adalah С 12 H 22 O 11 . Contoh umum adalah sukrosa (dibentuk oleh glukosa dan fruktosa), laktosa (dibentuk oleh galaktosa dan glukosa), dan maltosa (dibentuk oleh dua monomer glukosa).
- Trisakarida:
Mereka mengandung tiga monomer, misalnya rafinosa, rabinosa, rhaminosa, dll.
- Tetrasakarida:
Ini mengandung empat molekul monosakarida seperti stachyose dan scordose.
- Pentasakarida:
Ini memiliki lima monomer, misalnya verbascose.
[III] Polisakarida:
Ini adalah gula kompleks yang dibentuk oleh kondensasi banyak molekul monosakarida dengan hilangnya jumlah molekul air yang sama. Rumus empiris mereka adalah setelah hidrolisis, mereka menghasilkan molekul gula sederhana yang selanjutnya dapat berdisosiasi menjadi monomer. Secara struktural, mereka adalah molekul berukuran koloid yang memiliki berat molekul tinggi. Mereka terdiri dari dua jenis—
- Homopolisakarida:
Polisakarida ini mengandung sejenis monomer dalam molekulnya. Homopolisakarida yang umum adalah (i) pati, (ii) glikogen dan (iii) selulosa.
(a) Pati:
Ini adalah bahan makanan penyimpanan penting dari sel tanaman yang terjadi dalam matriksnya sebagai butiran. Secara struktural, itu terdiri dari dua molekul polimer panjang di antaranya rantai linier amilosa, dan amilopektin bercabang.
(b) Glikogen:
Itu terkandung terutama dalam sel hati hewan dan serat otot. Ini mudah larut dalam air tetapi membentuk suspensi koloid dengan protoplasma. Tidak seperti pati, itu disimpan makanan dalam sel hewan. Glikogen terdiri dari banyak molekul glukosa atau polimer glukosa.
(c) Selulosa:
Ini adalah karakteristik dinding sel tumbuhan yang memberikan dukungan mekanis pada sel. Selulosa adalah polimer gula-selobiosa diasakarida (С 12 H 22 O 11 ) yang mungkin mengandung banyak molekul glukosa.
- Heteropolisakarida:
Ini terdiri dari berbagai jenis molekul monosakarida. Dalam molekulnya, asam amino nitrogen sulfat atau fosfat adalah umum. Heteropolisakarida yang umum adalah sebagai berikut—
(a) Heteropolisakarida netral:
Mereka dikenal sebagai asetil glukosamin dan mengandung monosakarida dan nitrogen amino asetat. Contohnya adalah kitin yang membentuk kerangka luar serangga, dll.
(b) Heteropolisakarida asam:
Polisakarida ini mengandung berbagai jenis monosakarida dengan asam sulfat atau asam fosoforik dalam molekulnya. Di dalamnya termasuk asam hialuronat, heparin, kondroitin sulfat, dll. Heparin adalah antikoagulan darah yang ditemukan di hati, paru-paru, timus, darah.
Asam hialuronat membentuk bahan penyemen jaringan ikat dan terdapat di kulit, jaringan ikat, dan cairan sinovial sendi. Asam hialuronat dihidrolisis oleh hyaluronidase. Kondroitin sulfat ditemukan dalam sel tulang rawan, kornea, tali pusat dan berfungsi sebagai matriks untuk pembentukan tulang.
(c) Mukoprotein dan Glikoprotein:
Di dalamnya, molekul protein, monosakarida, dan asetil glukosamin bersatu membentuk mukoprotein dan glikoprotein yang khas. Contohnya adalah musin lambung, serum, albumin, polisakarida golongan darah.
3. Lipid:
Ini (Gr., liposâ €”lemak) adalah lemak yang terbuat dari С, H dan O. Mereka juga merupakan koloid yang tidak larut dalam air tetapi larut dalam pelarut organik seperti eter, kloroform, benzena, dll. Sifat lipid dan senyawa terkait ini adalah dominasi rantai hidrokarbon alifatik panjang atau cincin benzena. Struktur ini non-polar dan hidrofobik.
Dalam banyak lipid, rantai ini dapat melekat pada satu ujung ke gugus polar yang membuatnya mampu mengikat air dengan ikatan hidrogen. Lipid adalah konstituen penting dari membran sel, vitamin dan hormon sel. Ini hadir sebagai produk penyimpanan yang memasok energi. Mereka terdiri dari beberapa jenis—
[I] Lipid sederhana:
Trigliserida:
Ini adalah lemak netral, terdiri dari asam lemak dan gliserol sebagai trigliserida. Gliserida ini dapat berupa minyak atau lemak. Ini termasuk minyak lemak dan lemak babi — hati ikan kod dan minyak jarak. Pada hidrolisis mereka menghasilkan satu molekul gliserol dan 3 molekul asam lemak. Lemak netral menumpuk di jaringan adiposa.
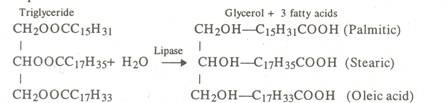
Asam lemak dapat jenuh (misalnya asam palmitat, stearat) atau tidak jenuh seperti asam oleat, linoleat, linolenat, dll. Sel-sel hewan mengandung asam palmitat, stearat, palmitoleat, oleat, linoleat dan linolenat. Lipid sederhana dari sitoplasma sel adalah lemak netral yang ditemukan dalam sel tumbuhan dan hewan sebagai zat makanan yang disimpan, dan lilin yang merupakan ester asam lemak dengan berat molekul tinggi dengan alkohol selain gliserol (misalnya lilin lebah).
Lilin memiliki titik leleh yang lebih tinggi daripada lemak netral. Misalnya, lilin lebah terutama terdiri dari asam palmitat yang diesterifikasi dengan hexacosonol atau triacontanol. Lilin bersifat inert secara kimiawi dan membentuk penutup pelindung di berbagai lokasi dalam sel.
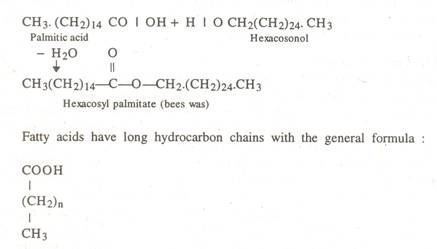
Asam lemak selalu memiliki jumlah karbon yang genap. Misalnya asam palmitat memiliki 16 karbon dan asam stearat memiliki 18 karbon. Terkadang rantai hidrokarbon memiliki ikatan rangkap (—С = С—), dan dalam hal ini asam lemak dikatakan tidak jenuh, misalnya asam oleat memiliki 18 karbon dan satu rangkap (tidak jenuh) menjalin kedekatan.
Gugus karboksil asam lemak bereaksi dengan gugus alkohol gliserol dengan cara berikut—
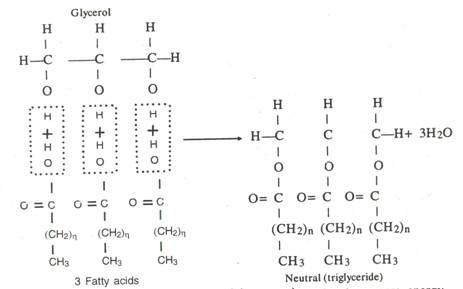
Trigliserida yang dihasilkan digunakan oleh organisme untuk menyimpan energi cadangan. Mereka melepaskan energi dalam jumlah besar, yaitu sekitar dua kali lipat dari karbohidrat dan protein, karena oksidasinya sangat lambat. Setelah oksidasi mereka membentuk CO 2 dan air.
[II] Lipid kompleks:
Lipid senyawa ini mengandung asam lemak, alkohol bersama dengan senyawa spesifik lainnya seperti fosfor, nitrogen amino, nerrone, dll. Setelah hidrolisis, lipid ini menghasilkan senyawa lain selain alkohol dan asam. Mereka berfungsi sebagai komponen struktural sel, terutama di membran sel. Mereka mungkin dari tipe berikut—
- Fosfolipid (Fosfatida):
Mereka adalah diester asam fosfat dan mengandung gliserol, asam lemak, dan asam fosfat dalam molekulnya. Fosfolipid adalah komponen utama membran unit sel dan mengatur permeabilitas sel, pembekuan darah, transportasi dan metabolisme lemak makanan.
Fosfolipid hanya memiliki dua asam lemak yang terikat pada molekul gliserol. Gugus hidroksil ketiga dari gliserol diesterifikasi menjadi asam fosfat, bukan menjadi asam lemak. Fosfat ini juga terikat pada molekul alkohol kedua, yang dapat berupa kolin, etanolamin, inositol atau serin tergantung pada jenis fosfolipidnya. Mereka dibagi lagi ke dalam kategori- kategori berikut—
(a) Lecithin:
Di dalamnya, fosfolipid disatukan dengan basa nitrogen—kolin dan karenanya disebut juga fosfatidil kolin. Ini adalah monoamino-mono-fosfolipid yang mengandung gliserol, asam lemak, asam fosfat dan kolin. Di jaringan saraf, fosfolipid terjadi bersama dengan kolesterol. Asam lemak yang ditemukan dalam lesitin termasuk asam palmitat, asam stearat, asam oleat, asam arakidonat, dan asam linoleat. Biasanya, hanya dua asam lemak yang terdapat dalam satu molekul lesitin.
Lesitin tidak stabil karena adanya asam lemak tak jenuh dan mengalami oksidasi atau hidrogenasi. Mereka memainkan peran penting dalam metabolisme lemak, permeabilitas, ketegangan osmotik, desaturasi lemak dan proses metabolisme lainnya.
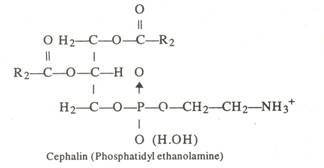
(b) Sefalitis:
Mereka terdiri dari fosfatidil etanolamin dan serin fosfatidil. Dengan kata lain, gugus kolin lesitin digantikan oleh gugus amino-etanol (P-amino-etanol atau serin). Cephalin membentuk komponen lipoprotein tertentu dan berperan penting dalam pembekuan darah.
(c) Plasmalogen:
Dalam fosfolipid ini, terjadi bentuk aldehida rantai panjang yang dihubungkan oleh ikatan ester. Plasmalogen mirip dengan lesitin tetapi salah satu asam lemaknya diganti.
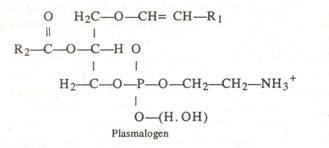
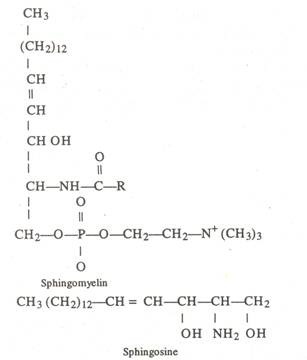
(d) Spingolipid:
Ini ditemukan sebagian besar di sel-sel otak. Di dalamnya, alih-alih gliserol, ada alkohol amino, yang disebut sphingol atau sphingosine. Selubung mielin serabut saraf mengandung lipid—sphingomyelin yang terbentuk dari sphingosine dan fosfolipid. Sphingolipid juga disebut sphingomyelins.
- Glikolipid:
Mereka mirip dengan sphingolipid tetapi mengandung radikal karbohidrat bersama dengan nitrogen dan asam lemak. Matriks sel hewan terdiri dari dua macam glikolipid yaitu serebrosida dan gangliosida.
(a) Serebrosida:
Mereka mengandung sphingosine, asam lemak dan galaktosa atau glukosa dalam molekulnya dan merupakan karakteristik dari materi putih sel otak dan selubung mielin. Cerebrosides umum adalah kerasin, cerebron, nervon, oxynervons dan phrenosin.
(b) Gangliosida:
Ini juga merupakan molekul kompleks yang terdiri dari sphingosine, asam lemak dan satu atau lebih molekul glukosa, laktosa, galaktosamin dan asam neuraminic. Mereka ditemukan di materi abu-abu otak, membran eritrosit dan sel limpa.
Pasang sulfa mengandung asam sulfat yang diesterifikasi menjadi galaktosa.
- Lipoprotein:
Ini mengandung protein dan lipid dalam molekulnya dan ditemukan dalam darah mamalia. Di dalamnya kolesterol dan protein globulin spesifik.
[III] Lipid turunan:
Setelah hidrolisis, lipid turunan menghasilkan lipid sederhana dan kompleks bersama dengan zat lain seperti aldehida lemak, hidrokarbon, sterid, keton, alkohol, dll. Jenisnya adalah sebagai berikut-
- Sterid:
Ini adalah lipid seperti lilin yang ditemukan di Free State serta membentuk ester asam lemak. Mereka dicirikan oleh adanya struktur cincin dalam molekulnya. Sterid terbagi dalam dua kategori yaitu steroid dan sterol.
(a) Steroid:
Ini adalah lipid yang lebih rumit yang mengandung inti cincin alifatik dari hidrokarbon jenuh. Dengan kata lain, ini adalah alkohol aromatik yang memiliki gugus OH. Cincin siklik adalah siklopentano perhidro-fenantrena. Pada sel tumbuhan, terdapat sterol-β-sitosterol yang khas, dan pada jamur, ergosterol (salah satu provitamin D). Mereka termasuk hormon seks, vitamin D dan asam empedu.
(b) Sterol:
Steroid yang memiliki gugus hidroksil (OH) dalam molekulnya disebut sterol. Sterol terjadi pada minyak dan lemak hewan dan tumbuhan. Contohnya adalah ergosterol dari ragi, kolesterol dari hewan dan ergosterol, stigmasterol dari tumbuhan. Mereka adalah alkohol padat seperti lilin yang ditemukan di sebagian besar sel hidup.
[IV] Karotenoid:
Ini adalah pigmen merah atau oranye dalam sel yang tidak larut dalam air tetapi larut dalam pelarut organik (misalnya vitamin-A-karoten). Formula umumnya adalah C 40 H 56 . Ada sekitar tujuh puluh karotenoid yang ditemukan di sel tumbuhan dan hewan. Diantaranya adalah termasuk karoten, xantofil, retinen, laktoflavin dalam susu, riboflavin (vitamin B 2 ), xanthocyanin, koenzim, anthocyanin, flavon, flavonol, flavonon, dll.
Karoten adalah jenis α, β dan γ; di antara P karoten mensintesis vitamin A. Xanthophylls memiliki С, H dan О sebagai lutein, pigmen daun kuning. Secara kimia karotenoid adalah porfirin (Gr. porphyra—ungu). Porfirin yang berikatan dengan logam dan protein membentuk pigmen penting sel hewan dan tumbuhan (misalnya, klorofil dan hemoglobin).
4. Enzim:
[I] Struktur enzim:
Ini adalah protein kompleks yang ditemukan dalam protoplasma yang bersifat koloid. Enzim ini bertindak sebagai biocatalyzer (katalisator biologis) dalam berbagai proses metabolisme dan dengan demikian mempercepat proses tersebut.
Katalis adalah zat yang mempercepat reaksi kimia tetapi tidak dimodifikasi sendiri dalam prosesnya, sehingga dapat digunakan berulang kali. Enzim adalah kelas molekul protein terbesar dan terspesialisasi. Lebih dari seribu enzim yang berbeda telah diidentifikasi.
Banyak dari mereka telah diperoleh dalam kondisi murni, dan bahkan kristal. Enzim mewakili salah satu produk terpenting dari gen yang diperoleh dalam molekul DNA. Enzim mungkin intraseluler (yaitu, bertindak di dalam sel) atau ekstraseluler (yaitu, bereaksi dalam media eksternal). Enzim adalah sub-negara tertentu, yaitu, enzim tertentu akan bekerja hanya pada substrat tertentu.
Beberapa enzim memiliki spesifisitas yang hampir mutlak untuk substrat tertentu dan tidak akan bekerja bahkan pada molekul yang sangat erat hubungannya, seperti stereoisomer dari molekul yang sama. Enzim lain memiliki spesifisitas relatif, karena mereka tidak akan bekerja pada berbagai senyawa terkait.
Beberapa enzim memerlukan komponen non-protein kecil yang disebut kofaktor untuk aktivitasnya. Misalnya, beberapa enzim adalah protein terkonjugasi yang memiliki gugus prostetik yang terikat erat, seperti dalam kasus sitokrom, yang memiliki kompleks besi porfirin. Atom besi sangat penting dalam banyak reaksi transfer-elektron.
Enzim lain tidak dapat berfungsi tanpa penambahan molekul kecil yang disebut koenzim, yang terikat selama reaksi. Ketika bergabung dengan koenzim, enzim yang tidak aktif ini, juga disebut apoenzim, membentuk holoenzim aktif.
Misalnya, dehidrogenase menggunakan nikotinamid—adenin dinukleotida (NAD + ) atau nikotinamid—adenin dinukleotida fosfat (NADP + ). Ini adalah salah satu koenzim yang paling penting. Fungsi koenzim adalah menerima dua elektron dan satu ion hidrogen dari substrat, sehingga mengoksidasinya —
Substrat + NAD + + Enzim → Substrat teroksidasi + NADH + H +
Dua elektron NADH kemudian dapat ditransfer ke molekul kedua, yang akan tereduksi, yaitu memperoleh elektron.
Di dalam sel, enzim katabolik penghasil energi menggunakan NAD sebagai koenzim dalam proses sintetik, namun menggunakan NADPH sebagai donor hidrogen. Pada banyak koenzim, seperti pada NAD + dan NADP + yang mengandung nikotinamid, komponen esensialnya adalah vitamin dari gugus Ð’. Enzim adalah zat yang tidak stabil yang dapat dihancurkan oleh suhu yang lebih tinggi.
Umumnya ini tetap dalam keadaan tidak aktif dan diaktifkan oleh zat lain. Misalnya tripsinogen, enzim yang tidak aktif, diaktifkan oleh enzim enterokinase di usus menjadi tripsin yang aktif.
Tripsinogen (tidak aktif) enterokinase →Tripsin (aktif)
[II] Klasifikasi enzim:
Enzim telah diklasifikasikan ke dalam enam kategori menurut terminologi terbaru seperti yang dijelaskan oleh De Robertis (1971). Mereka adalah—
(1) Oxidoreductases, melakukan reaksi oksidasi-reduksi sel; misalnya, hidrogenase (reduktase), oksidase, oksigenase dan peroksidase.
(2) Transferases, yang menyebabkan terjadinya perpindahan golongan.
(3) Hidrolase, yang menghidrolisis reaksi.
(4) Lisis, menyebabkan penambahan atau penghilangan gugus ke atau dari ikatan rangkap.
(5) Isomerase, yang mengkatalisis isomerisasi, dan
(6) Ligase atau sintetase, yang memadatkan dua molekul dengan memisahkan ikatan fosfat. Selain itu, ada isoenzim yang memiliki aksi serupa tetapi konfigurasi strukturalnya berbeda. Isoenzim ini dihasilkan oleh perubahan genetik. Ini memiliki hubungan dengan hereditas (Latner dan Skillen, 1969, dan Weyer, 1968). Ada sekitar 100 isoenzim di dalam sel.
[III] Cara kerja enzim:
Menurut konsep aktivitas enzim saat ini, enzim dan substrat (zat yang bekerja dengan enzim) membentuk hubungan kunci dan kunci. Di dalamnya, substrat menempel pada komponen protein enzim, yang disebut situs aktif.
Situs enzim ini berhubungan langsung dengan struktur protein primer (kadang-kadang sekunder dan tersier) karena berkaitan dengan urutan asam amino khusus. Baru-baru ini, sebuah konsep baru yang disebut induced-fit telah didalilkan oleh Koshland (1960) dan Yankeelov (1965).
Situs aktif bukanlah struktur yang kaku. Pada beberapa enzim, sisi aktif justru saling melengkapi dengan substrat hanya setelah substrat terikat, sebuah fenomena yang disebut induced-fit. Pengikatan substrat menginduksi perubahan konformasi pada protein dan hanya dengan demikian gugus kimia esensial untuk katalisis akan bersentuhan erat dengan substrat.
Pengikatan substrat ke situs aktif melibatkan kekuatan yang bersifat non-kovalen, yang jangkauannya sangat pendek. Hal ini menjelaskan mengapa kompleks enzim-substrat dapat dibentuk hanya jika enzim memiliki situs yang persis komplementer dengan bentuk substrat.
Keberadaan kompleks enzim-substrat (ES) di situs aktif dipostulasikan oleh Michaelis dan Menten (1913) berdasarkan bukti kinetik.
Reaksi enzim-substrat berlangsung dalam dua langkah:
(1) Langkah pertama adalah sebagai berikut.
Enzim + Substrat → Kompleks Enzim- Substrat (ES)
E + SK 1 ↔ K 2 (ES)
(2) Pada langkah kedua kompleks (ES) terurai untuk membentuk produk dan enzim bebas, yang sekarang akan tersedia untuk memproses molekul substrat baru.
(ES) K 3 †” K 4 E + P
K 1, K 2, K 3, dan K 4, adalah tetapan laju reaksi. Semua langkah dapat dibalik, tetapi secara umum K4 dapat diabaikan dan berikut ini—
(ES) → E+P
Sebagaimana terbukti kecepatan reaksi enzim tergantung pada konsentrasi substrat.
Pada konsentrasi substrat rendah, kecepatan awal meningkat dengan cepat. Di sini jumlah produk yang terbentuk sebanding dengan konsentrasi substrat , (S). Namun, ketika substrat meningkat, reaksi menjadi jenuh dan mencapai titik kesetimbangan di mana kecepatan tidak lagi bergantung pada (S). Pada titik ini, karena kelebihan besar substrat, semua enzim dalam bentuk kompleks (ES), dan kecepatan maksimum reaksi tercapai.
Koenzim:
Beberapa enzim memerlukan komponen non-protein kecil yang disebut kofaktor untuk aktivitasnya. Senyawa ini terikat pada protein. Kofaktor juga disebut gugus prostetik yang terikat sangat erat oleh ikatan kovalen dengan protein enzim. Enzim semacam itu disebut koenzim. Banyak enzim membutuhkan ion logam untuk aktivitas penuh, misalnya Mg ++ dan Mn ++ .
Bagian protein dari enzim disebut apoenzim dan enzim lengkap sering disebut holoenzim. Nicotinamide—adenine dinucleotide (NAD) atau nicotinamide—adenine dinucleotide phosphate (NADP) adalah koenzim yang penting.
Fungsi koenzim adalah menerima dua elektron dan ion hidrogen dari substrat, sehingga mengoksidasinya. Dalam banyak koenzim (seperti pada NAD dan NADP), komponen esensialnya adalah vitamin, khususnya pada gugus Ð’.
Isoenzim:
Isoenzim adalah beberapa bentuk enzim yang berbeda dengan variasi kecil dalam komposisi asam amino dan kadang-kadang dalam regulasi. Misalnya, lactic dehydrogenase (LDH), yang mengkatalisis konversi piruvat menjadi laktat.
5. Zat Pengatur:
Ini juga merupakan sekresi organik kompleks yang menjaga laju metabolisme sel secara teratur. Ini termasuk hormon dan vitamin.
[I] Hormon:
Hormon adalah sekresi protoplasma sel endokrin yang merupakan kelenjar tanpa saluran. Ini diproduksi dalam jumlah yang sangat kecil dan dituangkan ke dalam darah yang membawanya ke organ yang membutuhkan.
Hormon yang ada dalam sitoplasma sel mengatur sintesis m-RNA, enzim, dan berbagai aktivitas fisiologis intraseluler lainnya. Ini diproduksi oleh kelenjar yang berbeda. Kelenjar hipofisis, yang biasa disebut ‘kelenjar utama orkestra endokrin, mengeluarkan sekitar selusin hormon.
Di antaranya, somatotrofik mempengaruhi pertumbuhan; hipofisis mempengaruhi kelenjar susu, vasopresin untuk tekanan pembuluh darah, gonadotrofik untuk mengendalikan gonad, tirotrofik untuk mengendalikan kelenjar tiroid. Dengan demikian, ia mengontrol setiap bagian tubuh.
Hormon lainnya adalah tiroksin yang disekresikan oleh kelenjar tiroid yang memberikan energi; kortin yang disekresikan oleh korteks adrenal menjaga keseimbangan garam dalam darah, dll., dan adrenalin yang disekresikan oleh medula adrenal efektif pada otot tak sadar.
Hormon gonadial dapat berupa androgen atau estrogen, yang mengontrol perkembangan organ seks dan karakter seksual sekunder. Pada serangga, hormon ecdysone ditemukan membentuk cincin Balbiani pada kromosom raksasa. Ini juga mengontrol molting dan metamorfosis pada serangga (Beermann, 1965).
[II] Vitamin:
Vitamin sebenarnya tidak ada dalam sitoplasma tetapi diperoleh sel dari lingkungannya bersama dengan makanan, dll. Vitamin sangat penting untuk pertumbuhan normal, metabolisme, dan pemeliharaan kekuatan. Kekurangan vitamin mengurangi laju metabolisme sel dan dapat menyebabkan penyakit defisiensi. Vitamin ini mungkin banyak jenisnya, beberapa yang penting adalah sebagai berikut—
1.Vitamin A:
Ini melawan makhluk hidup terhadap infeksi dan membentuk ungu visual di retina. Kekurangannya menyebabkan rabun senja pada manusia. Itu hadir dalam karoten.
- Vitamin Ð’ (Kompleks):
Itu terbuat dari beberapa vitamin seperti vitamin Ð’ 1 , Ð’ 6 , B 12 , dll. Vitamin B 1 sangat penting untuk metabolisme karbohidrat dan respirasi jaringan yang tepat. Kekurangannya menyebabkan penyakit beri-beri (penyakit saraf). Vitamin B2 juga penting untuk pertumbuhan. Vitamin Ð’ 6 sangat penting untuk sintesis protein dan menyebabkan anemia. Vitamin Ð’ 12 bermanfaat untuk pembentukan sel darah merah pada manusia.
3.Vitamin C:
Ini larut dalam air, ditemukan dalam tomat, dll, dan berguna dalam respirasi jaringan, pertumbuhan normal tulang dan gigi. Kekurangannya menyebabkan penyakit kudis di mana tulang menjadi lemah dan kulit menjadi kasar.
4.Vitamin D:
Ini larut dalam lemak dan sangat penting untuk penyerapan kalsium dan fosfor, sehingga membantu dalam pembentukan tulang. Kekurangannya menyebabkan kerusakan gigi dan deformasi tulang.
5.Vitamin E:
Ini penting untuk pertumbuhan sel yang cepat dan kekurangannya menyebabkan kematian embrio dan kemandulan.
6.Vitamin K:
Ini membantu dalam pembentukan protrombin protein darah dan kekurangannya menyebabkan perdarahan karena darah gagal membeku.
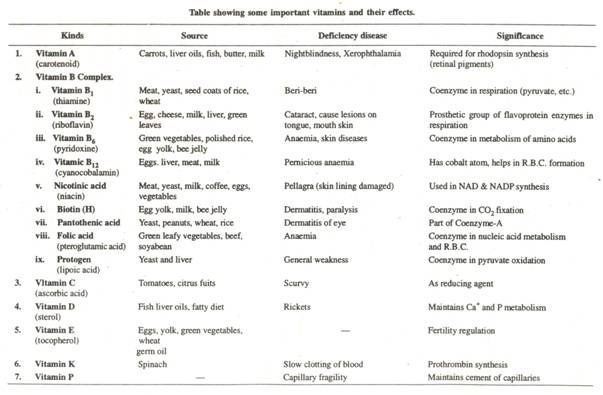
7.Vitamin P:
Ini adalah campuran eriodictin, hesperidin dan rutin, dan mempertahankan semen dinding kapiler, sehingga mempengaruhi kerapuhan kapiler.
6. Asam Nukleat:
Ini adalah zat organik penting yang ditemukan dalam nukleus dan sitoplasma. Mereka mengontrol aktivitas biosintetik penting sel dan membawa informasi herediter dari generasi ke generasi. Jadi, asam nukleat adalah makromolekul yang sangat penting secara biologis.
Mereka terkait dengan kromosom dan mengirimkan berbagai informasi ke sitoplasma. Asam nukleat ini ada dua jenis: (i) asam deoksiribonukleat (DNA) dan (ii) asam ribonukleat (RNA). DNA adalah penyimpan utama informasi genetik. Informasi ini ditransmisikan oleh transkripsi menjadi molekul RNA, yang digunakan dalam sintesis protein.
DNA→RNA→ Protein
Pada sel yang lebih tinggi, DNA terlokalisasi terutama di nukleus sebagai bagian dari kromosom. Sejumlah kecil DNA hadir dalam sitoplasma yang terkandung dalam mitokondria dan kloroplas. RNA ditemukan baik di dalam nukleus, di mana ia disintesis, dan di dalam sitoplasma, di mana sintesis protein berlangsung. Kedua jenis asam nukleat adalah polimer nukleotida. Nukleotida terbuat dari nukleosida dan asam fosfat.
Nukleosida terbentuk dari gula pentosa (ribosa atau deoksiribosa) dan basa nitrogen (purin dan pirimidin). Purin adalah adenin dan guanin, dan pirimidin adalah sitosin, timin, dan urasil. Sitoplasma hanya mengandung RNA, dan DNA secara eksklusif ditemukan dalam nukleus. Setelah hidrolisis ringan, asam nukleat didekomposisi menjadi nukleotida.